Résistance à l'acide nucléique de Mycobacterium tuberculosis et à la rifampicine
Nom du produit
HWTS-RT074B - Kit de détection de l'acide nucléique de Mycobacterium tuberculosis et de la résistance à la rifampicine (courbe de fusion)
Certificat
CE
Épidémiologie
Mycobacterium tuberculosis, abrégé en bacille de la tuberculose, est la bactérie pathogène responsable de la tuberculose. Actuellement, les antituberculeux de première intention couramment utilisés comprennent l'isoniazide, la rifampicine et l'hexambutol. Les antituberculeux de deuxième intention comprennent les fluoroquinolones, l'amikacine et la kanamycine. Parmi les nouveaux médicaments développés figurent le linézolide, la bédaquiline et le delamani. Cependant, en raison d'une utilisation inappropriée des antituberculeux et des caractéristiques de la structure de la paroi cellulaire de Mycobacterium tuberculosis, cette bactérie développe une résistance aux médicaments, ce qui représente un défi majeur pour la prévention et le traitement de la tuberculose.
La rifampicine est largement utilisée dans le traitement de la tuberculose pulmonaire depuis la fin des années 1970 et s'avère très efficace. Elle constitue le traitement de première intention pour raccourcir la chimiothérapie chez les patients atteints de tuberculose pulmonaire. La résistance à la rifampicine est principalement due à la mutation du gène rpoB. Bien que de nouveaux antituberculeux soient régulièrement mis sur le marché et que l'efficacité clinique du traitement de la tuberculose pulmonaire continue de s'améliorer, le nombre de médicaments disponibles reste relativement limité, et le recours inapproprié aux antituberculeux demeure fréquent. De toute évidence, l'éradication complète et rapide de Mycobacterium tuberculosis chez les patients atteints de tuberculose pulmonaire entraîne une résistance variable aux médicaments, prolonge la durée de la maladie et augmente le risque de décès.
Canal
| Canal | Canaux et fluorophores | Tampon de réaction A | Tampon de réaction B | Tampon de réaction C |
| Chaîne FAM | Journaliste : FAM, Quencher : Aucun | rpoB 507-514 | rpoB 513-520 | 38KD et IS6110 |
| Chaîne CY5 | Journaliste : CY5, Quencher : Aucun | rpoB 520-527 | rpoB 527-533 | / |
| Canal HEX (VIC) | Journaliste : HEX (VIC), Quencher : Aucun | Contrôle interne | Contrôle interne | Contrôle interne |
Paramètres techniques
| Stockage | ≤-18℃ Dans l'obscurité |
| durée de conservation | 12 mois |
| Type de spécimen | Expectorations |
| CV | ≤5,0% |
| LoD | Mycobacterium tuberculosis 50 bactéries/mL souche sauvage résistante à la rifampicine : 2 x 103bactéries/mL mutant homozygote : 2x103bactéries/mL |
| Spécificité | Il détecte le mycobacterium tuberculosis de type sauvage et les sites de mutation d'autres gènes de résistance aux médicaments tels que katG 315G>C\A, InhA-15C> T ; les résultats du test ne montrent aucune résistance à la rifampicine, ce qui signifie qu'il n'y a pas de réactivité croisée. |
| Instruments applicables : | Systèmes PCR en temps réel SLAN-96P Système PCR en temps réel BioRad CFX96 Système PCR en temps réel LightCycler480® |
Flux de travail
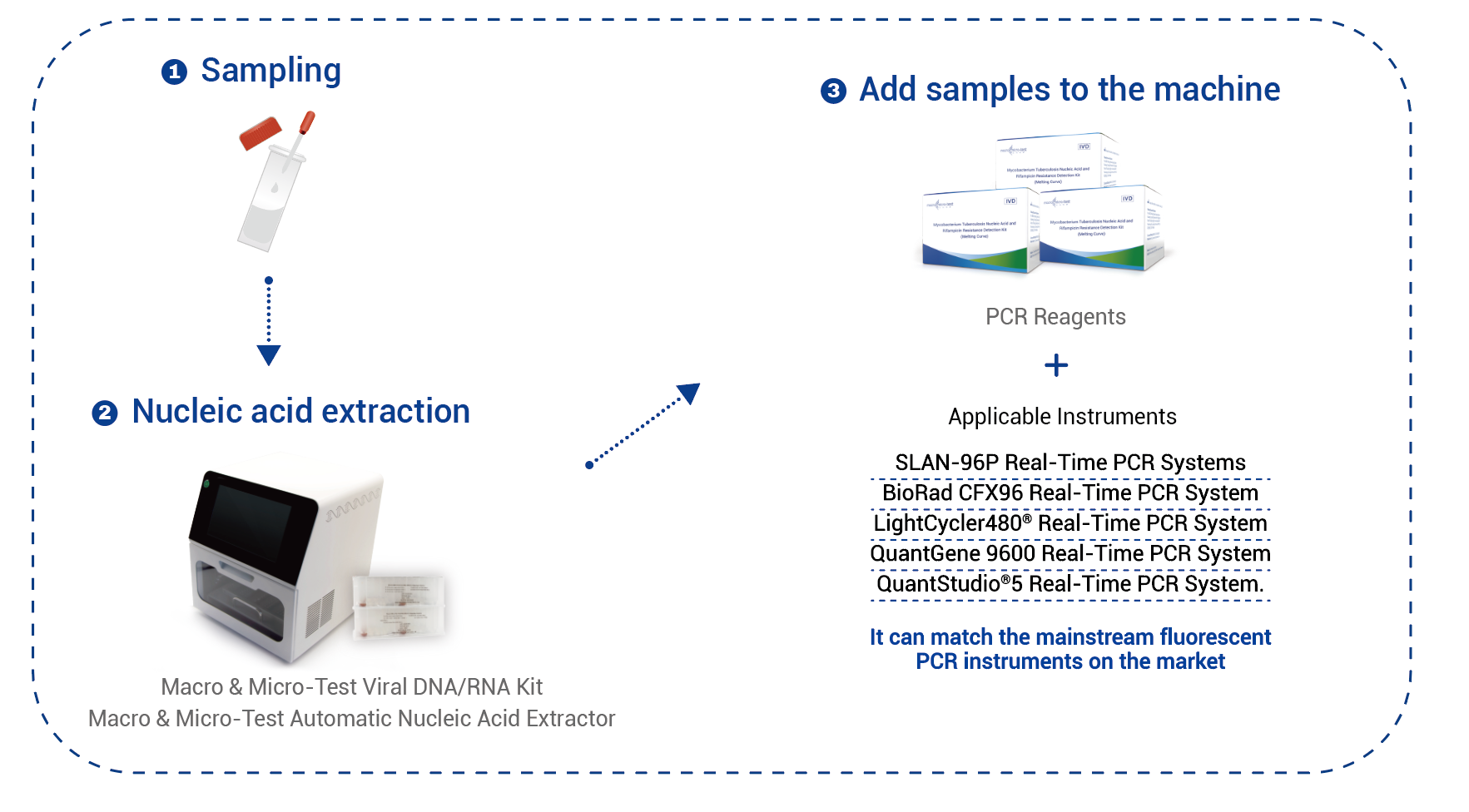
Si vous utilisez le kit d'extraction d'ADN/ARN général Macro & Micro-Test (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (compatible avec l'extracteur automatique d'acides nucléiques Macro & Micro-Test (HWTS-3006C, HWTS-3006B)) ou la colonne d'extraction d'ADN/ARN viral Macro & Micro-Test (HWTS-3022-50) de Jiangsu Macro & Micro-Test Med-Tech Co., Ltd., ajoutez successivement 200 μL de contrôle positif, de contrôle négatif et d'échantillon d'expectorations traité à tester, puis 10 μL de contrôle interne séparément à chacun de ces éléments. Les étapes suivantes doivent être réalisées en suivant scrupuleusement les instructions d'extraction. Le volume d'échantillon extrait est de 200 μL et le volume d'élution recommandé est de 100 μL.