I. Aperçu duESMOLignes directrices pour 2025
En août 2025, l'ESMO a officiellement publié les Recommandations de pratique clinique de l'ESMO pour le diagnostic, le traitement et le suivi du cancer du poumon non à petites cellules de stade précoce et localement avancé, dans la revue d'oncologie de référence Annals of Oncology. Il s'agit de la première mise à jour complète depuis la version de 2017, qui constitue une référence incontournable pour les oncologues du monde entier.

Le cancer du poumon présente l'incidence et la mortalité les plus élevées de tous les cancers à l'échelle mondiale. Chaque année, on dénombre plus de 2,2 millions de nouveaux cas et plus de 1,8 million de décès, ce qui en fait la première cause de mortalité par cancer chez les hommes et les femmes. Le cancer du poumon non à petites cellules (CPNPC) représente environ 80 à 85 % des cas de cancer du poumon. Face à ce grave constat, la publication des recommandations de 2025 insuffle une nouvelle dynamique scientifique à la pratique clinique, la mise à jour des stratégies de dépistage des biomarqueurs étant particulièrement cruciale.
II. Interprétation des principales mises à jour des lignes directrices
2.1 Tests de biomarqueurs : d’« optionnel » à « essentiel »
Les recommandations de 2025 constituent un ajustement stratégique majeur concernant les tests de biomarqueurs. Elles stipulent explicitement que ces tests sont essentiels pour la décision thérapeutique chez les patients atteints d'un cancer du poumon non à petites cellules de stade IB à III.
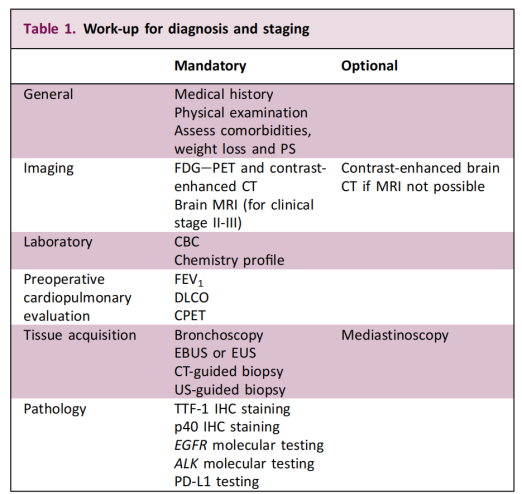
Cette recommandation étend l'utilisation des tests moléculaires, auparavant réservés aux patients atteints d'une maladie avancée, aux cas précoces résécables. L'objectif principal est d'identifier les mutations des gènes moteurs et de fournir une base scientifique pour un traitement de précision personnalisé. La recommandation souligne également que la faisabilité de la biopsie et la stratégie diagnostique doivent être déterminées par une équipe multidisciplinaire en fonction des caractéristiques du patient et de la tumeur.
Concernant la stratégie de dépistage, les recommandations préconisent clairement la réalisation de tests génétiques avant toute décision chirurgicale, incluant au minimum les gènes EGFR et ALK. Ce concept de « dépistage précoce » revêt une importance clinique majeure pour la stratification précise et le traitement personnalisé du cancer bronchique non à petites cellules (CBNPC) de stade précoce : la rapidité et la fiabilité des résultats déterminent directement le choix du traitement adjuvant ultérieur.
2.2 Avancées thérapeutiques dans le CBNPC de stade précoce positif à l'oncogène conducteur
Les lignes directrices de 2025 intègrent les données probantes de plusieurs études cliniques majeures afin d'établir un parcours de traitement de précision clair pour les patients atteints d'un CBNPC de stade précoce positif à un oncogène moteur.
Patients porteurs de la mutation EGFR :S’appuyant sur l’étude ADAURA, une étude de référence, l’osimertinib adjuvant postopératoire pendant trois ans est devenu le traitement de référence mondial pour les patients présentant une délétion de l’exon 19 ou une mutation L858R de l’exon 21 du gène EGFR. L’étude ADAURA est une étude internationale, multicentrique, randomisée et contrôlée de phase III évaluant l’efficacité et la tolérance de l’osimertinib adjuvant chez les patients atteints d’un cancer bronchique non à petites cellules (CBNPC) de stade IB à IIIA, porteur d’une mutation de l’EGFR et ayant subi une résection complète. Cette étude a démontré que l’osimertinib améliorait significativement la survie sans progression et la survie globale par rapport au placebo, faisant de l’osimertinib le nouveau traitement de référence pour cette population. Cependant, des analyses exploratoires de l’étude ADAURA ont indiqué qu’environ 36 % des arrêts précoces de traitement étaient dus à des événements indésirables et 31 % à la décision du patient. Ce constat souligne la nécessité de réaliser des tests initiaux précis avant le traitement afin de garantir que la thérapie ciblée soit administrée aux patients susceptibles d’en tirer un bénéfice durable.
Patients ALK-positifs :D’après l’étude ALINA, l’alectinib adjuvant postopératoire pendant deux ans constitue désormais le traitement de référence. Dans l’analyse principale de l’étude ALINA de phase III, randomisée et ouverte, l’alectinib a démontré un bénéfice marqué en termes de survie sans progression (SSP) chez les patients atteints d’un cancer bronchique non à petites cellules (CBNPC) de stade II-IIIA, avec un rapport de risque (RR) de 0,24. Les données actualisées de l’étude ALINA, présentées au congrès ESMO 2025, ont montré qu’après un suivi d’au moins trois ans, le bénéfice de l’alectinib en termes de SSP restait durable et cliniquement significatif, avec un RR de 0,36 chez les patients atteints d’un CBNPC de stade II-IIIA. Le taux de survie globale à quatre ans, le plus récent, a atteint 98,4 %, le taux de SSP à quatre ans était de 75,5 % et la SSP du système nerveux central était également améliorée, sans nouveau signal de sécurité. Ces données robustes confirment l’alectinib adjuvant comme traitement de référence après résection d’un CBNPC ALK-positif et soulignent l’importance d’un dépistage précis pour identifier ces patients.
Choix de la méthode d'essai :Les lignes directrices de l'ESMO de 2025 listent explicitementTests RT-PCR multiplex sur panelOutre le séquençage de nouvelle génération (NGS) basé sur l'ARN, l'immunohistochimie (IHC) et l'hybridation in situ en fluorescence (FISH), cette approche technique est recommandée pour la détection de la fusion ALK. Cela indique que l'objectif principal de cette recommandation est de réaliser des tests pour orienter les décisions cliniques, plutôt que d'imposer une plateforme de test spécifique. Pour les produits RT-PCR ciblant la détection des gènes EGFR et ALK, cette stratégie de test flexible justifie pleinement leur utilisation en pratique clinique, conformément aux recommandations.
III. Solutions techniques de test de précision
La recommandation de 2025 étend les tests à la phase préopératoire, ce qui rehausse les exigences en matière de précision, de sensibilité et d'accessibilité des analyses. Les deux produits de détection par RT-PCR décrits ci-dessous répondent parfaitement aux exigences techniques de cette recommandation.
3.1 Kit de détection des mutations de l'EGFR – Plateforme technologique ARMS améliorée
Technologie de baseLa technologie ARMS améliorée permet l'amplification spécifique de séquences mutantes peu abondantes sur un fond de séquences sauvages abondantes.
Trois garanties techniques:
-ARMS amélioré → améliore la reconnaissance des mutations
- Enrichissement enzymatique → digère le matériel génétique sauvage et enrichit les séquences mutantes
- Le blocage thermique → supprime l'amplification non spécifique
Performance: Sensibilité defréquence de l'allèle mutant de 1 %
Contrôle de la contaminationContrôle interne intégré + enzyme UNG pour prévenir la contamination
délai de traitementFonctionnement en tube fermé, environ120 minutes
Compatibilité des échantillons:Tissu/biopsie liquideexemples → répond à l'exigence de « tests préalables »
Couverture:45 mutationsdans les exons 18 à 21 de l'EGFR, correspondant précisément aux régions mises en évidence par les directives (délétions de l'exon 19 et L858R de l'exon 21)
Utilisation clinique: Guide directement le traitement par inhibiteurs de tyrosine kinase de l'EGFR
Kit de détection de fusion EML4-ALK 3,2 MMT – Solution de détection de fusion basée sur l'ARN

-Plateforme technologiqueLa RT-PCR basée sur l'ARN offre des avantages intrinsèques par rapport aux méthodes basées sur l'ADN pour la détection des fusions.
-Avantage basé sur l'ARNDétecte directement les transcrits de fusion exprimés, évitant ainsi efficacement les faux négatifs.
-Preuves de l'étudeDans les cas de fusions ALK peu abondantes, la RT-PCR est nettement plus fiable que les tests basés sur l'ADN.
-Sensibilité: Détecte les fusions jusqu'à20 copies par réaction
-Couverture des variantes: Couvertures12 variantes courantes de fusion EML4-ALK(dont la variante 1 ~33%; les variantes 3a/3b ensemble ~29%)
-Contrôle des opérations et de la contaminationTube fermé, environ 120 minutes ; contrôles de processus intégrés et enzyme UNG pour éviter les faux résultats
-Compatibilité des instrumentsCompatible avec divers instruments de PCR en temps réel courants
-Alignement des lignes directrices: Tout à fait conforme aux recommandations de l'ESMO
IV. Cohérence entre les analyses et les recommandations des lignes directrices
Les deux produits de détection sont parfaitement conformes aux recommandations ESMO 2025 sur le cancer du poumon non à petites cellules de stade précoce et localement avancé, selon les dimensions clés suivantes :
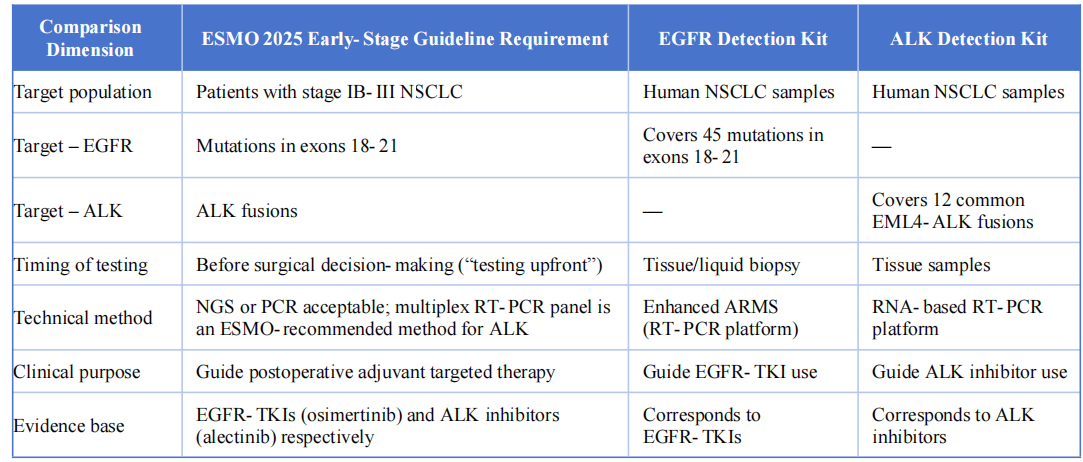
V. Conclusion
Les recommandations ESMO 2025 sur le cancer du poumon non à petites cellules de stade précoce inaugurent une nouvelle ère de diagnostic et de traitement de précision, axée sur «tests préalables, ciblage précis et optimisation du traitement.« Les kits de détection des mutations EGFR et de fusion MMT EML4-ALK répondent aux exigences des directives en matière de cibles, de délais et de précision grâce à des approches techniques distinctes. »
Le kit EGFR utilise une technologie ARMS améliorée pour la détection à haute sensibilité des mutations ciblées dans des échantillons limités, prenant en charge à la fois la biopsie tissulaire et la biopsie liquide pour permettre un « test en amont ».
Le kit ALK est basé sur la RT-PCR à base d'ARN, offrant des avantages par rapport aux méthodes ADN pour la détection de fusion, conformément à la recommandation de l'ESMO concernant les panels RT-PCR multiplex pour les tests ALK.
Ensemble, ces deux produits constituent une solution de test de précision conforme aux directives ESMO 2025, soutenant une thérapie adjuvante personnalisée pour le CBNPC de stade précoce.
Références :
- Zer A, Ahn MJ, Barlesi F, et al. Cancer du poumon non à petites cellules de stade précoce et localement avancé : recommandations de pratique clinique de l’ESMO pour le diagnostic, le traitement et le suivi. Ann Oncol. 2025 ;36(11) :1245-1262. doi :10.1016/j.annonc.2025.08.003
Date de publication : 6 mai 2026

