Le 24 mars 2026 marquera la 31e Journée mondiale de la tuberculose. L’Organisation mondiale de la Santé (OMS) a annoncé que le thème mondial de cette année sera :« Oui ! Nous pouvons éradiquer la tuberculose ! », soulignant qu’un leadership gouvernemental fort, un engagement politique soutenu et une action multisectorielle coordonnée sont essentiels pour mettre fin à l’épidémie de tuberculose (TB).

Progrès mondiaux et défis restants
Selon le Rapport mondial sur la tuberculose 2025, la lutte mondiale contre la tuberculose a franchi une étape importante en 2024, avec à la fois iL'incidence et la mortalité sont en baissepour la première fois depuis la pandémie de COVID-19.
Une estimation10,7 millions de personnesEn 2024, 54 % des cas de tuberculose ont été recensés, dont 54 % chez les hommes, 35 % chez les femmes et 11 % chez les enfants et les adolescents. Parmi ces cas, environ619 000 (5,8 %)étaient co-infectés par le VIH, et390 000 (3,6 %)étaient des tuberculoses multirésistantes ou résistantes à la rifampicine (TB-MR/RR).
La tuberculose a causé environ1,23 million de mortsEn 2024, la tuberculose est restée la principale cause infectieuse de décès dans le monde, dépassant la COVID-19. Après trois années d'augmentation entre 2021 et 2023, l'incidence mondiale de la tuberculose a diminué de près de 2 % en 2024, reflétant une reprise progressive des services de lutte contre la tuberculose.[1]
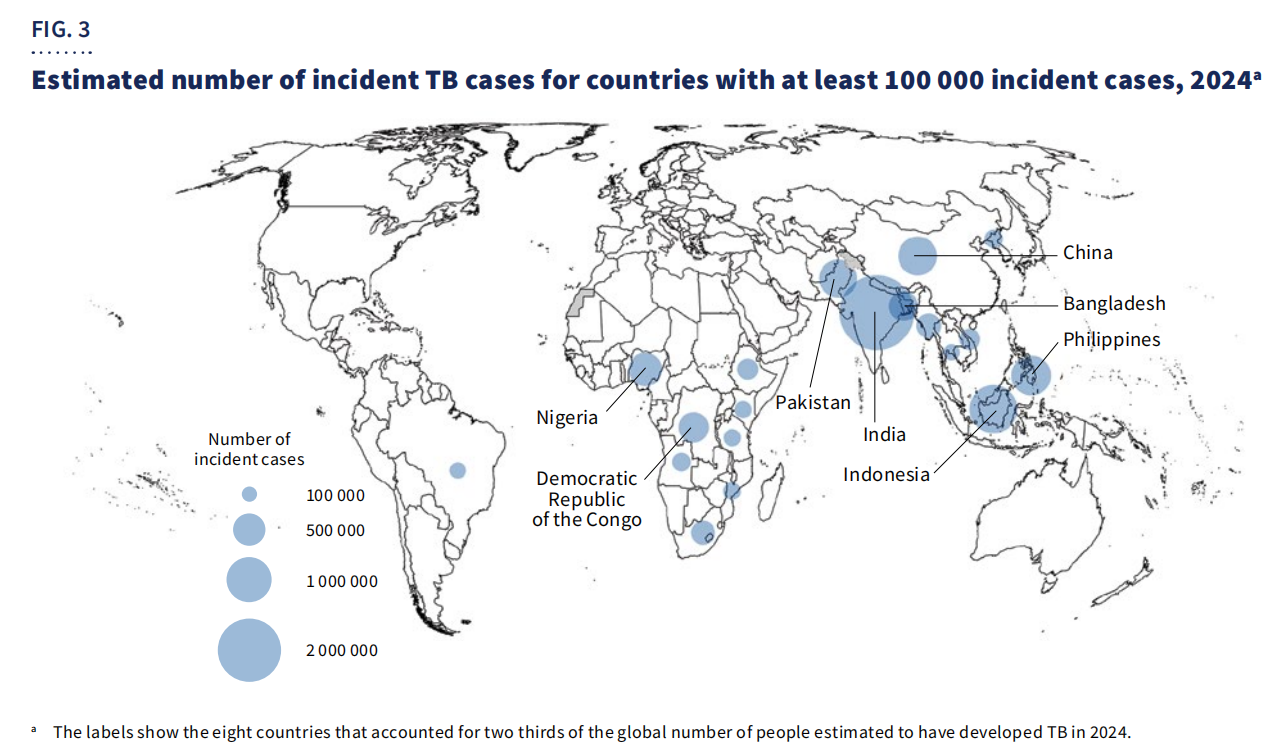
Géographiquement,67 % des casétaient concentrées dans huit pays : l’Inde, l’Indonésie, les Philippines, la Chine, le Pakistan, le Nigéria, la République démocratique du Congo et le Bangladesh.
Malgré les progrès accomplis, la tuberculose demeure une cause majeure de décès chez les personnes vivant avec le VIH et contribue fortement à la mortalité liée à la résistance aux antimicrobiens. Le financement mondial reste insuffisant, avec seulement5,9 milliards de dollars américainsdisponible en 2024, bien en dessous duObjectif annuel de 22 milliards de dollars américainsprévu pour 2027.
Ces chiffres soulignent l’urgence de renforcer les programmes de lutte contre la tuberculose à l’échelle mondiale, en mettant l’accent sur l’élargissement de l’accès aux diagnostics, l’amélioration des résultats des traitements et la prise en compte des déterminants sociaux qui favorisent la transmission de la tuberculose. La lutte contre la tuberculose exige toujours une coopération internationale et un engagement politique solides pour atteindre les objectifs de la Stratégie pour mettre fin à la tuberculose.
Mycobacterium tuberculosis : Pathogénie et classification
Mycobacterium tuberculosis (MTB/M. tuberculosis) est le principal agent pathogène responsable de la tuberculose (TB). Il peut pénétrer dans l'organisme par les voies respiratoires, le tube digestif ou par des lésions cutanées et muqueuses, infectant ainsi plusieurs organes et provoquant différentes formes de TB. La tuberculose pulmonaire, principalement transmise par les gouttelettes respiratoires, représente plus de 80 % des cas. Les symptômes courants incluent la toux, la production d'expectorations et l'hémoptysie. Après l'infection pulmonaire, la bactérie peut se propager par voie sanguine à d'autres systèmes, pouvant entraîner une tuberculose osseuse, urinaire ou gastro-intestinale.[2]
MTB fait partie du genre Mycobacterium, qui comprend :
- Complexe Mycobacterium tuberculosis (MTBC) : Il comprend notamment M. tuberculosis, M. bovis, M. africanum, M. canettii et M. microti. Si M. tuberculosis est la principale cause de la tuberculose, M. bovis et M. africanum peuvent également induire la maladie.
- Mycobactéries non tuberculeuses (MNT).
- Mycobacterium leprae, l'agent causal de la lèpre.
Approches diagnostiques de laboratoire
Un diagnostic précis et rapide est essentiel pour une lutte efficace contre la tuberculose. L'Organisation mondiale de la santé souligne queLes technologies de diagnostic moléculaire rapide ont fondamentalement transformé la détection de la tuberculose en permettant une identification très sensible et spécifique des agents pathogènes, tout en détectant simultanément la résistance aux médicaments.[1].
- Microscopie et culturee: La culture reste la méthode de référence pour le diagnostic de la tuberculose, car elle permet l'identification formelle des organismes viables et soutient les tests de sensibilité aux médicaments et l'analyse génomique. Cependant, en raison de la croissance lente de Mycobacterium tuberculosis, les résultats sont généralement obtenus sous 2 à 8 semaines, ce qui limite son utilité clinique dans la prise de décisions urgentes.
-Tests immunologiques: Les méthodes immunologiques, notamment le test cutané à la tuberculine (TST) et les tests de libération d'interféron gamma (IGRA), détectent les réponses immunitaires de l'hôte à l'infection tuberculeuse. Bien qu'utiles pour identifier une infection latente, ces tests ne permettent pas de distinguer avec certitude une infection active d'une infection ancienne et présentent donc une spécificité diagnostique limitée dans les régions à forte prévalence.
-Diagnostic moléculaire (NAAT): Les tests basés sur l'ADN, tels que l'amplification des acides nucléiques (NAAT), sont recommandés en raison de leur haute sensibilité et spécificité.
-Séquençage ciblé de nouvelle génération (tNGS): Les technologies de séquençage ciblé permettent une identification à haute résolution des mutations associées à la résistance. Les recommandations de l’OMS préconisent le séquençage ciblé de nouvelle génération (tNGS) comme outil avancé pour la détection de la résistance aux médicaments après le diagnostic, contribuant ainsi à l’élaboration de stratégies de traitement de précision [3].
-Séquençage métagénomique de nouvelle génération (mNGS): Le séquençage métagénomique permet la détection non biaisée d'un large éventail d'agents pathogènes sans sélection préalable de la cible. Cette approche est particulièrement précieuse dans les situations cliniques complexes ou ambiguës, notamment les infections mixtes et chez les patients immunodéprimés, où les méthodes diagnostiques conventionnelles peuvent s'avérer insuffisantes.
L’OMS souligne en outre que la confirmation microbiologique est essentielle pour initier un traitement approprié et améliorer les résultats des patients, renforçant ainsi l’importance d’intégrer les diagnostics moléculaires avancés dans les programmes de lutte contre la tuberculose [1].
Solutions complètes de diagnostic moléculaire de Macro & Micro-Test
1.Détection par PCR multiplex de la tuberculose et de la résistance aux médicamentsTB
| Code produit | Nom du produit | Certification |
| HWTS-RT001 | Kit de détection de l'ADN de Mycobacterium tuberculosis (PCR par fluorescence) | CE |
| HWTS-RT137 | Kit de détection des mutations de résistance à l'isoniazide chez Mycobacterium tuberculosis (courbe de fusion) | CE |
| HWTS-RT074 | Kit de détection de l'acide nucléique de Mycobacterium tuberculosis et de la résistance à la rifampicine (courbe de fusion) | CE |
| HWTS-RT102 | Kit de détection des acides nucléiques basé sur l'amplification isotherme par sonde enzymatique (EPIA) pour Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Kit de détection des acides nucléiques du complexe Mycobacterium tuberculosis lyophilisé (amplification isotherme par sonde enzymatique) | CE |
| HWTS-RT105 | Kit de détection d'ADN de Mycobacterium tuberculosis lyophilisé (PCR par fluorescence) | CE |
| HWTS-RT147 | Kit de détection de la résistance à l'acide nucléique de Mycobacterium tuberculosis et à la rifampicine et à l'isoniazide (courbe de fusion) | CE |
En cas de forte suspicion clinique de tuberculose (TB),HWTS-RT147Ce test est recommandé pour la détection qualitative de l'infection par le Mycobacterium tuberculosis (MTB) et de la tuberculose multirésistante (TB-MR). Ce test identifie les mutations du gène codant pour le MTB.gène rpoB, qui entraînent une résistance à la rifampicine (RIF) et des mutations dans leGènes katG et InhACe test, qui cible les souches de tuberculose associées à la résistance à l'isoniazide (INH), offre un diagnostic rapide et précis de la tuberculose multirésistante (TB-MR) et des infections à Mycobacterium tuberculosis (MTB). Il intègre un contrôle qualité interne afin de minimiser les faux négatifs et de garantir des résultats rapides et fiables.
2.Séquençage ciblé PTNseq pour les agents pathogènes respiratoires et profilage de la résistance
| Code produit | Nom du produit | Spécial. |
| HWKF-TS0001 | Kit d'enrichissement de gènes pathogènes pour les infections sanguines PTNseq | 24 tests/kit |
| HWKF-TS0002 | Kit d'enrichissement génique PTNseq pour les micro-organismes pathogènes responsables d'infections du système nerveux central | 24 tests/kit |
| HWKF-TS0003 | Kit d'enrichissement de gènes pathogènes pour les infections respiratoires PTNseq | 24 tests/kit |
| HWKF-AT0003 | Kit de construction de bibliothèque d'enrichissement automatisé pour les micro-organismes pathogènes des infections respiratoires PTNseq (ONT) | 24 tests/kit |
| HWKF-TS0004 | Kit d'enrichissement de gènes à large spectre pour agents pathogènes infectieux PTNseq | 24 tests/kit |
| HWKF-TS0005 | Kit d'enrichissement de gènes à très large spectre pour micro-organismes pathogènes infectieux PTNseq | 24 tests/kit |
| HWKF-TS0151 | Kit de typage des mycobactéries et d'enrichissement des gènes de résistance aux médicaments (méthode d'amplification multiple) | 24 tests/kit |
En cas d’infections respiratoires mixtes (y compris les infections des voies respiratoires supérieures et inférieures, la tuberculose et les maladies respiratoires chroniques), ou lorsqu’une analyse des gènes de résistance aux médicaments est nécessaire (par exemple, en cas de suspicion de tuberculose résistante aux médicaments),Série PTNseq de détection de gènes ciblée à haut débitCette méthode peut être appliquée. Basée sur une technologie de séquençage ciblé avancée, PTNseq utilise une PCR ultra-multiplex pour enrichir des séquences cibles spécifiques, combinée à un séquençage à haut débit et à une technologie nanopore de troisième génération pour une identification complète des agents pathogènes et un profilage de la résistance aux médicaments.
Le système utilise des amorces brevetées à haute spécificité pour l'amplification ultra-multiplexe des gènes cibles. S'appuyant sur une base de données propriétaire et des algorithmes bioinformatiques intelligents, il permet une identification précise des pathogènes ainsi que l'analyse des gènes de résistance aux médicaments et de virulence. L'enrichissement ciblé réduit les interférences de l'ADN hôte, améliorant la sensibilité dans les échantillons présentant un fort bruit de fond humain et permettant la détection efficace de cibles difficiles telles que…Mycobacterium tuberculosis, les champignons, les bactéries intracellulaires, les virus à ARN et les gènes de résistance ou de virulence.
PTNseq atteint une limite de détectionaussi peu que 100 copies/mLet couvre175 agents pathogènes respiratoires courants, dont 76 bactéries, 73 virus, 19 champignons, 7 mycoplasmes, ainsi queChlamydia, Rickettsiaet 54 gènes de résistance aux médicamentsLe panneau comprend leMycobacterium tuberculosismycobactéries non tuberculeuses complexes et majeures.
La gamme PTNseq allie haute sensibilité et rentabilité, améliorant ainsi les taux de détection des pathogènes et favorisant une antibiothérapie personnalisée tout en contribuant à limiter la résistance aux antimicrobiens. Intégrée au système entièrement automatisé de préparation des banques de séquençage génétique (AIOS), elle offre une solution hospitalière simplifiée avec un délai d'obtention des résultats de seulement 6,5 heures après prélèvement.

3. Séquençage métagénomique pour la détection d'agents pathogènes à large spectre
| Code produit | Nom du produit | Spécial. |
| HWKF-MN0011 | Kit de détection métagénomique des agents pathogènes (ADN-Illumina) | 24 tests/kit |
| HWKF-MN0018 | Kit de détection métagénomique des agents pathogènes (ADN-MGI) | 24 tests/kit |
| HWKF-MN0021 | Kit de détection métagénomique des agents pathogènes (ADN-ONT) | 24 tests/kit |
| HWKF-MN0012 | Kit de détection métagénomique des agents pathogènes (ARN-Illumina) | 24 tests/kit |
| HWKF-MN0019 | Kit de détection métagénomique des agents pathogènes (RNA-MGI) | 24 tests/kit |
| HWKF-MN0022 | Kit de détection métagénomique des agents pathogènes (RNA-ONT) | 24 tests/kit |
| HWKF-MN0013 | Kit de détection métagénomique des agents pathogènes (ADN+ARN-Illumina) | 24 tests/kit |
| HWKF-AYM0013 | Détection métagénomique des pathogènes, construction automatisée de bibliothèques KiT (ADN+ARN-Illumina) | 24 tests/kit |
| HWKF-MN0020 | Kit de détection métagénomique des pathogènes (ADN+ARN-MGI) | 24 tests/kit |
| HWKF-MN0023 | Kitt de détection métagénomique des agents pathogènes (ADN+ARN-ONT) | 24 tests/kit |
Lorsque le diagnostic clinique est incertain,détection à haut débit de gènes pathogènes par mNGSCette méthode peut être appliquée à divers échantillons prélevés chez le patient, notamment le liquide de lavage broncho-alvéolaire, les expectorations, les prélèvements de gorge, le sang, l'épanchement pleural, le pus et les échantillons tissulaires. Elle utilise la technologie de séquençage métagénomique, où différents échantillons subissent un prétraitement ciblé suivi d'une extraction d'acides nucléiques à l'aide de billes de verre et d'enzymes de digestion de la paroi cellulaire, ce qui améliore l'efficacité de l'extraction. Le séquençage est adapté à de multiples plateformes, garantissant un volume de données élevé pour une sensibilité accrue du séquençage métagénomique de nouvelle génération (mNGS) et une meilleure intégrité de l'assemblage. Les données sont analysées à l'aide d'une base de données développée spécifiquement pour cette étude et d'algorithmes intelligents pour la détection de pathologies.plus de 20 000 agents pathogènes, notamment les bactéries, les champignons, les virus et les parasites, fournissant des informations sur les micro-organismes pathogènes suspectés. Cette méthode est adaptée aux patients difficiles à diagnostiquer, gravement malades ou immunodéprimés, et permet notamment l'identification deVTTcomplexeetNTMainsi que pour les infections mixtes. Il améliore considérablement les taux de détection des agents pathogènes et contribue à orienter l'utilisation ciblée des antibiotiques, permettant ainsi un diagnostic précis de l'infection.
Conclusion
Malgré des progrès considérables, la tuberculose demeure un défi majeur pour la santé mondiale, notamment en raison de la résistance aux médicaments, des lacunes de financement et de l'accès inégal aux diagnostics.
L’OMS souligne que l’accès élargi aux tests de diagnostic moléculaire rapide et aux technologies de séquençage avancées est essentiel à la réalisation des objectifs de la Stratégie pour mettre fin à la tuberculose. Grâce à l’innovation continue, aux investissements et à la collaboration mondiale, l’élimination de la tuberculose n’est plus une aspiration, mais un objectif réalisable.
Références:
- Organisation mondiale de la santé. Rapport mondial sur la tuberculose 2024/2025 : Diagnostic et traitement.
- Organisation mondiale de la santé. Manuel de l'OMS pour la sélection des tests de diagnostic rapide moléculaires recommandés par l'OMS pour la détection de la tuberculose et de la tuberculose pharmacorésistante.
- Organisation mondiale de la santé. Directives consolidées de l'OMS sur la tuberculose : Module 3 – Diagnostic (mise à jour 2024).
Date de publication : 24 mars 2026
