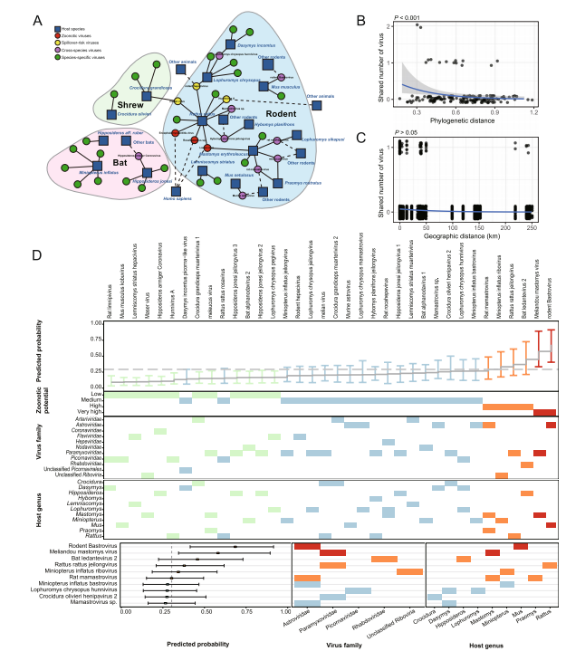
Une étude récente publiée dansMicrobiomeUne analyse métagénomique virale a été menée sur 846 petits mammifères sauvages (chauves-souris, rongeurs et musaraignes) collectés en Sierra Leone, en Afrique de l'Ouest. L'étude a permis d'identifier 39 virus à ARN associés aux mammifères, dont 26 nouveaux et 13 déjà connus. Parmi ceux-ci, la famille des Paramyxoviridae présentait la plus grande diversité, tandis que les rongeurs abritaient le plus grand nombre d'espèces virales (n = 26).
L'évaluation des risques zoonotiques a révélé la présence de trois virus zoonotiques connus — le virus de l'encéphalomyocardite, le virus Lassa et Rocahepevirus sp. — ainsi que de trois virus présentant un risque potentiel de transmission inter-espèces : le virus Melian, le virus de l'hépatite des rongeurs et le Hunnivirus A. Notamment, parmi les virus nouvellement identifiés, le ledantévirus 2 de la chauve-souris a montré la plus grande proximité phylogénétique avec le virus Le Dantec, responsable d'infections humaines. L'analyse sérologique a par ailleurs détecté des anticorps neutralisants contre ce virus chez 2,8 % des résidents locaux, suggérant une exposition humaine antérieure, probablement non détectée.
Ces résultats mettent en évidence l'existence d'un important réservoir viral, dominé par les rongeurs, en Afrique de l'Ouest et soulignent l'importance cruciale de stratégies de surveillance intégrées à l'interface homme-animal. L'association du criblage métagénomique à la validation sérologique constitue un cadre fiable pour l'identification des virus à potentiel zoonotique et de transmission inter-espèces.

Au cours de la dernière décennie, plus de 60 % des maladies infectieuses émergentes chez l'humain proviennent de réservoirs animaux, les chauves-souris, les rongeurs et les musaraignes étant reconnus comme des hôtes clés des virus zoonotiques. L'Afrique est largement considérée comme un foyer important de maladies zoonotiques. Par exemple, la Sierra Leone a recensé plus de 28 000 cas lors de l'épidémie d'Ebola de 2014-2016.
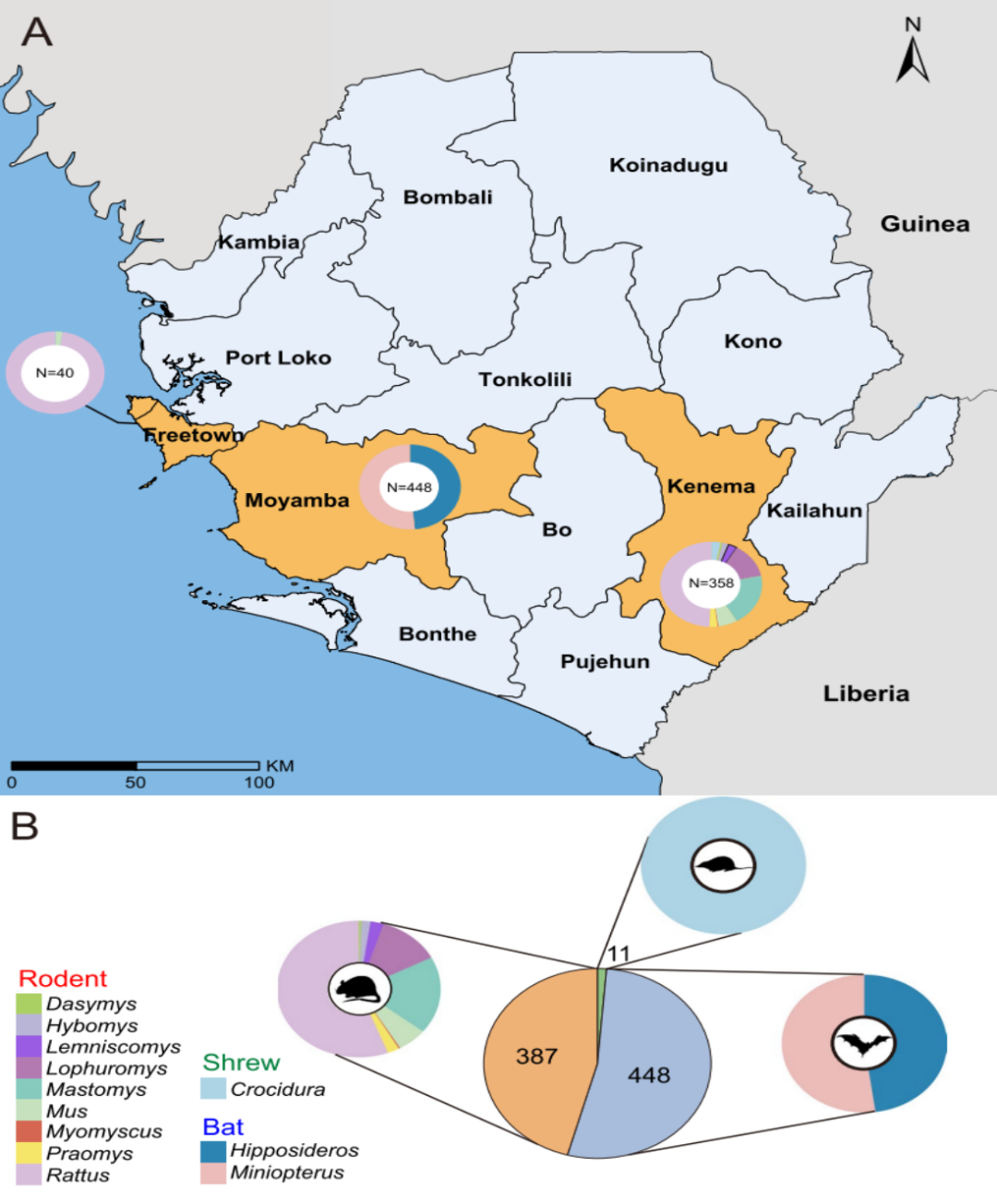
Malgré le fardeau important que représentent les zoonoses dans cette région, la diversité et la distribution des virus chez les petits mammifères sauvages restent insuffisamment caractérisées. Afin de combler cette lacune, des chercheurs ont mené une analyse virologique systématique de 846 petits mammifères sauvages capturés sur trois sites en Sierra Leone entre 2018 et 2023. L’étude visait à caractériser la diversité virale, à identifier les virus candidats à la transmission interspécifique, à évaluer le risque zoonotique et à fournir des données probantes pour étayer les systèmes d’alerte précoce aux maladies infectieuses émergentes.
Méthodes fondamentales
L'étude a appliqué un flux de travail complet de métagénomique virale :
- Traitement des échantillons :Des tissus cardiaques, hépatiques, spléniques, pulmonaires et rénaux ont été prélevés, regroupés, homogénéisés et soumis à une extraction d'ARN total.
- Séquençage et assemblage :L'élimination de l'ARN ribosomique a été réalisée avant la construction de la banque, suivie d'un séquençage à haut débit sur la plateforme Illumina NovaSeq 6000. Les contigs viraux ont été assemblés de novo.
- Identification du virus :Les virus ont été identifiés par alignement du gène de l'ARN polymérase ARN-dépendante (RdRp). Seuls les virus associés aux vertébrés ont été retenus, à l'exclusion des virus bactériens, fongiques et végétaux.
- Analyse bioinformatique :Une reconstruction phylogénétique, une analyse de recombinaison, une modélisation des réseaux de transmission inter-espèces et une évaluation des risques zoonotiques ont été réalisées.
- Validation sérologique :Un test de neutralisation de pseudovirus basé sur le VSV a été développé pour le ledantévirus 2 de la chauve-souris. Des anticorps neutralisants ont été détectés dans 2,8 % des sérums humains, ce qui prouve une transmission zoonotique potentielle.
ÉtudeRésultats
1. Découverte et diversité virales
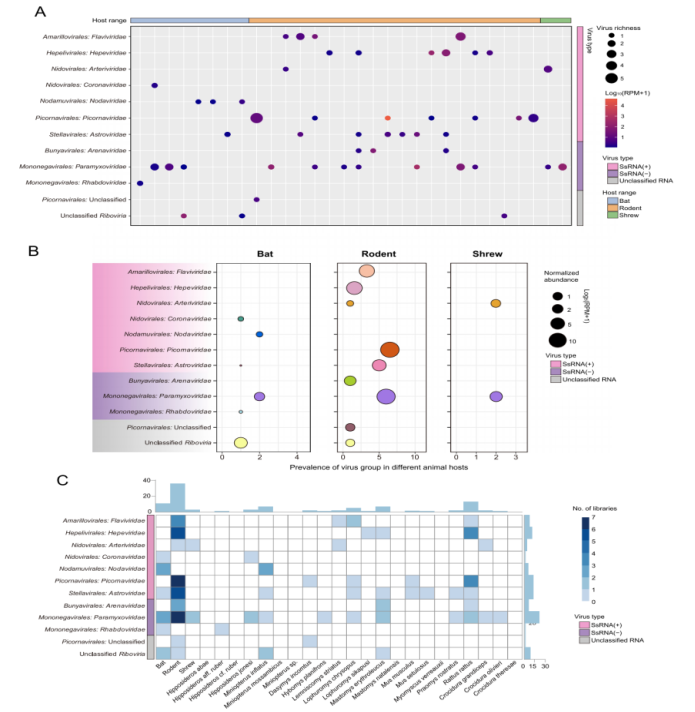
Cette étude a réalisé une analyse de séquençage transcriptomique sur 846 animaux sauvages collectés en Sierra Leone, notamment des rongeurs, des chauves-souris et des musaraignes. À partir des séquences complètes du gène de l'ARN polymérase ARN-dépendante (RdRp), un total de 39 virus à ARN associés aux mammifères ont été identifiés, dont 13 virus déjà connus et 26 nouveaux virus.
En termes de composition virale, la famille des Paramyxoviridae a présenté la plus grande diversité parmi les trois ordres d'hôtes, suivie des Astroviridae et des Picornaviridae. Concernant la distribution des hôtes, les rongeurs ont contribué à la plus grande diversité virale, abritant un total de 26 espèces virales, ce qui souligne leur rôle prépondérant de réservoirs de diversité virale dans la région.
2. Risque zoonotique
L’évaluation des risques zoonotiques a permis d’identifier trois virus zoonotiques connus : le virus de l’encéphalomyocardite, le virus Lassa et des espèces de Rocahepevirus. De plus, trois virus – le virus Melian, le virus de l’hépatite des rongeurs et le Hunnivirus A – ont été identifiés comme présentant un risque potentiel de transmission inter-espèces.
Parmi les 26 virus nouvellement découverts, quatre présentent un potentiel zoonotique élevé, prédit sur la base de leurs caractéristiques phylogénétiques et génomiques. Notamment, le bat ledantevirus 2 présente la plus grande proximité phylogénétique avec le virus Le Dantec, connu pour infecter l'homme.
Des analyses sérologiques ultérieures ont confirmé ce résultat, des anticorps neutralisants contre le ledantévirus 2 de chauve-souris ayant été détectés dans 2,8 % des sérums de résidents locaux. Ce résultat suggère que des infections non diagnostiquées ou asymptomatiques ont pu se produire au sein de la population humaine, mettant en évidence une voie de transmission zoonotique potentielle, mais jusqu'alors inconnue.
3. Dynamique de transmission inter-espèces
L'analyse de la transmission interspécifique a démontré que les rongeurs occupent une place centrale au sein du réseau de partage viral, jouant un rôle de nœud clé qui facilite les échanges viraux entre espèces hôtes. Au total, 15 virus ont été identifiés comme présentant un potentiel de transmission interspécifique.
Une analyse plus poussée des schémas de transmission inter-ordres a révélé que le partage viral était plus fréquent entre hôtes appartenant au même ordre taxonomique, ce qui suggère que la parenté entre hôtes joue un rôle important dans la dynamique de transmission. En revanche, les chauves-souris ont présenté une capacité de transmission inter-ordres relativement plus faible.
Il est important de noter que certains virus ont présenté une expansion de leur gamme d'hôtes. Par exemple, le virus Melian, auparavant considéré comme spécifique aux musaraignes, a également été détecté chez les rongeurs dans cette étude, ce qui indique une possible modification de son adaptabilité à différents hôtes et un risque accru de transmission à plus grande échelle.
Conclusions et implications pour la santé publique
- Grande diversité du virome chez les petits mammifères sauvages :La découverte de 39 virus à ARN, dont 26 nouvelles espèces, révèle un important réservoir de virus dans la région et signale pour la première fois de nouveaux virus à fort potentiel zoonotique (par exemple, le bat ledantevirus 2).
- Les rongeurs, cibles prioritaires de la surveillance :Les rongeurs jouent un rôle clé dans la transmission virale et présentent la plus grande diversité virale, ce qui représente le risque de transmission le plus élevé.
- Nécessité de stratégies de surveillance intégrées :Ces résultats plaident en faveur d’une priorisation des rongeurs dans les programmes de surveillance active et de la mise en œuvre d’approches intégrées combinant métagénomique, sérologie et surveillance écologique aux interfaces homme-faune.
Globalement, cette étude apporte des preuves essentielles à l'appui des systèmes d'alerte précoce et des cadres d'évaluation des risques liés aux maladies zoonotiques émergentes, renforçant ainsi l'importance d'une surveillance proactive dans les régions à haut risque.
Informations sur le produit
Date de publication : 23 mars 2026